近期,國外(wài)新冠肺炎持續爆發,對口罩等防疫物(wù)質需求大(dà)增,由于各國标準不同,我(wǒ)國出口非醫用口罩誤作醫用的情況時有發生(shēng)。3月31日,商(shāng)務部會同海關總署、藥監局發布《關于有序開(kāi)展醫療物(wù)資(zī)出口的公告》(2020年第5号),要求出口醫用口罩等5類産品必須取得國家藥品監管部門相關資(zī)質,符合進口國(地區)質量标準要求。
廣州進口報關公司
那麽,究竟如何快速準确地區分(fēn)醫用與非醫用口罩呢?請跟發布君一(yī)起來了解。
1、口罩的基本分(fēn)類與細分(fēn):口罩從用途可以分(fēn)爲醫用/非醫用兩大(dà)類。顧名思義,醫用口罩主要用于醫療方面的防護,可以細分(fēn)爲醫用防護、醫用外(wài)科、一(yī)次性醫用三種;非醫用口罩也被稱爲個人防護口罩,可根據其适用場景,可細分(fēn)爲防顆粒物(wù)和日常防護兩種。不同用途的口罩其技術要求不同、适用範圍也不同。
中(zhōng)國主要的口罩分(fēn)類
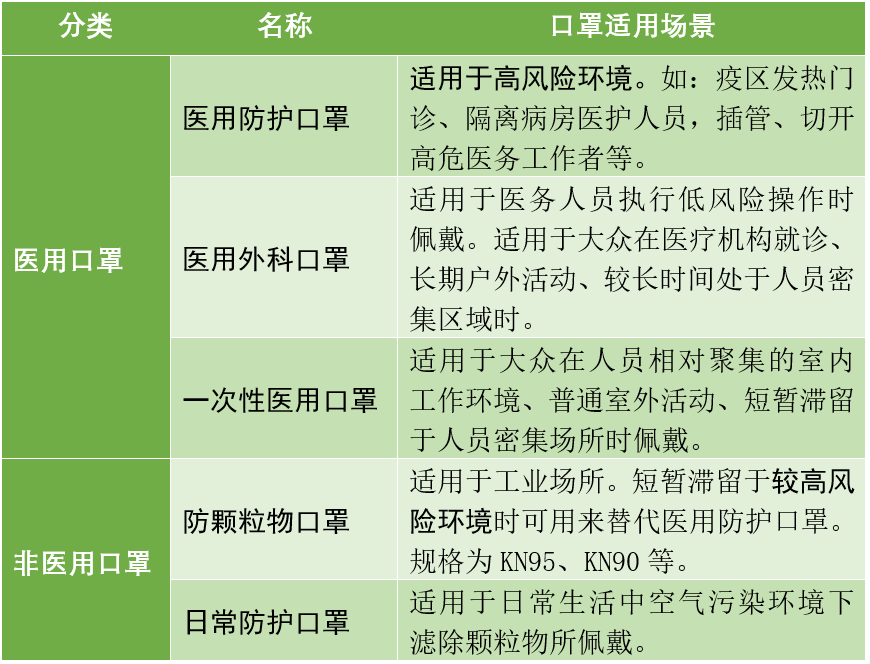 2、利用外(wài)觀與包裝信息區分(fēn)醫用/非醫用口罩
2、利用外(wài)觀與包裝信息區分(fēn)醫用/非醫用口罩
通過口罩結構區分(fēn)
通過過濾閥分(fēn)辨。帶過濾閥的口罩一(yī)般不會是醫用口罩。如中(zhōng)國醫用防護口罩标準GB 19803-2010 第4.3條款就明确規定“口罩不應有呼氣閥”,這樣可避免飛沫、微生(shēng)物(wù)等通過呼氣閥呼出,從而危害他人。而民用口罩允許有呼氣閥,通過呼氣閥可以減小(xiǎo)呼氣阻力,從而有利于作業人員(yuán)長時間工(gōng)作。
通過外(wài)包裝上的信息分(fēn)辨
正規途徑銷售的口罩産品的最小(xiǎo)單元包裝上應該有商(shāng)品名稱、執行的标準和防護等級等信息。這些商(shāng)家明示的信息可以作爲一(yī)個分(fēn)辨點,如商(shāng)品名稱中(zhōng)帶有“醫用”或英文“surgical”“Medical”等字樣的,一(yī)般可判定爲醫用口罩。
3、适用标準區分(fēn)醫用/非醫用口罩
醫用口罩在不同國家/地區适用不同的标準和認證要求,企業和個人可根據産品進口國家/地區,根據産品的适用标準進行區分(fēn),産品适用标準和認證信息可從産品外(wài)包裝或生(shēng)産者提供的檢測報告或證書(shū)獲得。
出口美國
醫用口罩在美國屬于醫療器械,适用《醫用口罩材料性能标準規範》(ASTM F2100),由美國食品藥品監督管理局(FDA)管理,須通過501K注冊或近期FDA公布的其它途徑,獲得工(gōng)廠注冊和醫療器械列名後方可在美國上市。因此,輸往美國的口罩外(wài)包裝或檢測報告或證書(shū)上有上述内容的,可被判定爲醫用口罩。出口美國非醫用口罩不屬2020年第5号公告範圍,但企業應注意,産品需通過NIOSH注冊方可在美國上市。
出口歐盟
歐盟醫用/非醫用口罩均需加貼CE标志(zhì),但适用标準不同。醫用口罩在歐盟屬于I類器械,分(fēn)爲I類非無菌和無菌兩種,需按照歐盟醫療器械指令93/42/EEC(MDD)或歐盟醫療器械條例EU2017/745(MDR)加貼CE标志(zhì),對應的标準是EN14683,輸往歐盟的口罩外(wài)包裝或檢測報告、證書(shū)上有上述内容的,可被判定爲醫用口罩。
需要注意的是,根據口罩無菌/非無菌狀态,歐盟采取不同的合格評定辦法,非無菌醫用口罩企業隻需進行CE自我(wǒ)符合性聲明,不需要通過公告機構認證。在準備好相應文件及測試報告等資(zī)料後,即可自行完成符合性聲明。無菌醫用口罩還必須由授權公告機構進行CE認證。出口歐盟非醫用口罩不屬于醫療器械,但需符合歐盟個人防護設備條例EU2016/425(PPE)要求,由授權公告機構進行CE認證并頒發證書(shū),對應的标準是EN149。
出口其它國家和地區
輸往其它國家和地區口罩産品,可參考其提供的中(zhōng)國标準檢測證書(shū)與注冊備案信息進行判斷,中(zhōng)國醫用口罩标準有三個,GB 19083-2010、YY 0469-2011、YY/T 0969-2013,使用這三個标準生(shēng)産的口罩可被判定爲醫用口罩。
本文鏈接
本站部分(fēn)素材來源于網絡,如有侵權請聯系本站客服删除!

